Une formulation optimisée pour la livraison de l'ARN messager
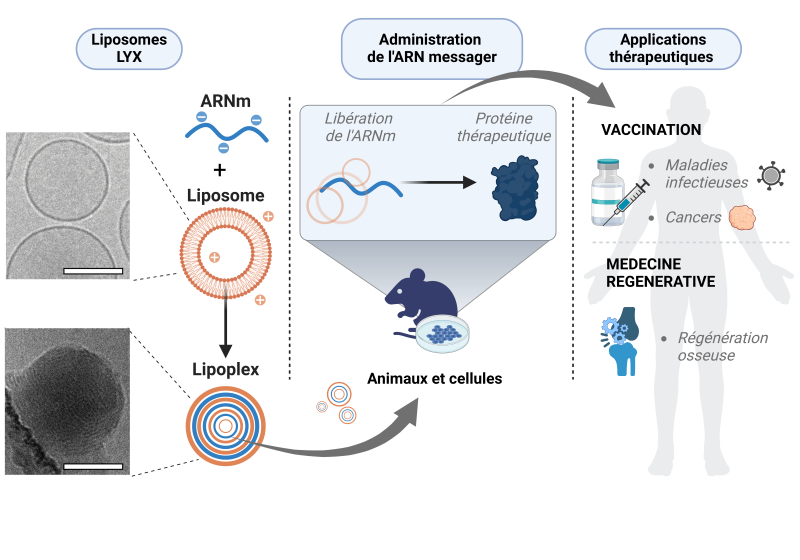
L'ARN messager est une molécule précieuse qui permet aux cellules de produire les protéines dont elles ont besoin. Mais pour l’utiliser à des fins thérapeutiques, il faut protéger cette molécule fragile en l’encapsulant pour la véhiculer jusqu’aux cellules. Les liposomes, petites capsules creuses faites de lipides, sont une solution très versatile. Des scientifiques ont mis au point une version optimisée de ces capsules, baptisée LYX, qui offre un nouvel élan aux thérapies à ARNm.
L’ARN messager (ARNm) est une molécule biologique qui joue un rôle clé dans le fonctionnement des cellules. C’est lui qui porte les instructions pour fabriquer les protéines essentielles à l’organisme. Il s’agit également d’une molécule au potentiel thérapeutique immense, comme l’ont montré les vaccins contre le COVID19. Introduit artificiellement dans la cellule, il lui permet de fabriquer elle-même des protéines thérapeutiques, ce qui en fait un outil prometteur pour traiter de nombreuses maladies. Mais une difficulté majeure subsiste : comment faire entrer efficacement cet ARNm dans les cellules sans qu'il soit dégradé en chemin ?
L’ARNm est en effet une molécule très fragile. Injecté dans le corps, il est rapidement dégradé, notamment par des enzymes, avant même d’atteindre sa cible. Pour éviter cela, les scientifiques ont développé des moyens de l’encapsuler pour l’acheminer efficacement vers les cellules, soit dans des nanoparticules, soit dans des liposomes. Ces derniers sont de minuscules capsules constituées de lipides, semblables aux membranes cellulaires, qui sont facilement absorbées dans les cellules. Contrairement aux nanoparticules lipidiques, ils sont simples à fabriquer. Mais le contrôle de leur taille et leur stabilité reste un défi.
Dans ce contexte, une équipe du Centre de biophysique moléculaire d’Orléans (CNRS), en collaboration avec le laboratoire Biologie, bioingénierie et bioimagerie ostéo-articulaires (CNRS/INSERM/Université Paris Cité), a mis au point une nouvelle version améliorée de ces véhicules, appelée LYX. En incluant une étape de lyophilisation et d’extrusion au procédé de fabrication de ces liposomes, les scientifiques sont parvenus à contrôler parfaitement leur taille et augmenter leur stabilité. Les liposomes ainsi obtenus se distinguent également par leur capacité à libérer leur chargement de manière plus efficace dans les cellules. En laboratoire, ces liposomes ont démontré une excellente résistance, pouvant être stockés pendant un an tout en conservant leurs propriétés. Leur structure optimisée favorise l’absorption cellulaire et une libération progressive de l'ARN dans le cytoplasme.
Les tests menés sur des cellules et sur des modèles animaux montrent notamment que LYX peut transporter de l'ARNm codant pour des protéines thérapeutiques impliquées dans la régénération osseuse. Une fois dans les cellules, ces liposomes assurent la production de ces protéines en quantités suffisantes pour induire une réponse biologique significative. En prime, lorsqu'ils sont intégrés dans des hydrogels implantables, ils conservent leur capacité à libérer l'ARN in vivo, une étape cruciale vers des applications cliniques.
Ces résultats, publiés dans le Journal of Controlled Release, ouvrent de nouvelles perspectives pour les thérapies à ARNm. Si des améliorations restent à apporter pour renforcer leur efficacité sur les cellules à cibler et limiter certains effets indésirables, cette stratégie permettra d'améliorer les vaccins ou encore de réparer des tissus endommagés.
Rédacteur : AVR
Référence
Structural and functional characterization of a histidylated liposome for mRNA delivery
Albert Ngalle Loth, Manon Maroquenne, Ayoub Medjmedj, Franck Coste, Thomas Bizien, Chantal Pichon, Delphine Logeart-Avramoglou & Federico Perche
Journal of Controlled Release 2025
https://doi.org/10.1016/j.jconrel.2025.01.010