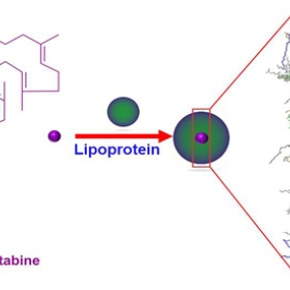
Vectorisation indirecte d'anticancéreux par les lipoprotéines
Les chercheurs de l’Institut Galien (Université Paris-Sud/ Université Paris-Saclay) ont découvert qu’il était possible d’exploiter les lipoprotéines circulant naturellement dans le sang pour augmenter l’efficacité de principes actifs anticancéreux, à condition que ceux-ci soient dotés de groupements chimiques présentant une forte affinité spécifique pour les lipoprotéines. Ces travaux sont publiés dans la revue Nature Communications et ont été réalisés dans le cadre de l’ERC Advanced Grant « TERNANOMED ».
La gemcitabine est un médicament largement utilisé pour le traitement de divers cancers. Seule, elle est rapidement métabolisée dans le sang et son efficacité est de courte durée. Dans une précédente étude, les chercheurs de l’Institut Galien ont montré qu’il était possible d’augmenter la durée de vie de ce principe actif en le couplant au squalène, un lipide naturel et biocompatible. Ils ont ensuite observé l’auto-assemblage des deux molécules en milieu aqueux pour former des nanoparticules. Ce couplage offre une activité antitumorale bien supérieure à la gemcitabine utilisée seule, grâce à une pharmacocinétique prolongée. Comment expliquer cette augmentation de la durée de vie du principe actif dans le sang ?
C’est le caractère lipidique du squalène et sa proximité structurale avec le cholestérol (dont il est le précurseur chez les mammifères) qui ont convaincu les chercheurs de l’Institut Galien de s’intéresser à la possible interaction entre ces nanoparticules et les lipoprotéines plasmatiques, le squalène, pouvant, au même titre que le cholestérol, présenter une forte affinité pour celles-ci. Il a été montré in vitro sur sang humain et in vivo chez l’animal que les bioconjugués de gemcitabine-squalène sont rapidement captés par les lipoprotéines circulantes (LDL chez l’homme et HDL chez le rongeur) après désagrégation des nanoparticules dans la circulation sanguine. Cette affinité pour les lipoprotéines a un caractère général car elle a également été démontrée avec d’autres bioconjugués squalénés. L’interaction entre les nanoparticules squalénées et les LDL peut être imaginée comme un processus dynamique qui implique l’adsorption des petites particules de LDL (22 nm) à la surface des nanoparticules (120 nm) dès qu’elles entrent en contact les unes avec les autres, comme cela a été montré en microscopie électronique à transmission.
Mieux encore ! Les chercheurs ont constaté que l’insertion de la gemcitabine-squalène dans les LDL augmentait fortement la capture par les cellules cancéreuses car celles-ci sont équipées de récepteurs capables de reconnaitre spécifiquement les LDL. L’approche suivie pourrait donc avoir des implications importantes pour le traitement du cancer en ciblant plus spécifiquement les cellules malades.
Ainsi, en provoquant l’insertion de médicaments in situ en présence de squalène, directement dans les LDL circulants, les chercheurs ont mis en évidence un nouveau concept, celui de la “vectorisation indirecte” de médicaments.
![]()
Référence
Sobot D, Mura S, Yesylevsky S, Dalbin L, Cayre F, Bort G, Mougin J, Desmaele D, Lepetre-Mouelhi S, Pieters G, Andreiuk B, Klymchenko A, Paul J-L, Ramseyer C & Couvreur P
Conjugation of squalene to gemcitabine as unique approach exploiting endogenous lipoproteins for drug delivery
Nature Communications 30 mai 2017
doi: 10.1038/ncomms15678