Une nouvelle étape pour la redox anionique
Les piles et les batteries reposent sur des échanges d’électrons qui ont lieu lors de l’oxydation et la réduction d’ions positifs. L’implication des ions négatifs (redox anionique) permettrait de doubler les performances, mais provoque une dégradation du matériau trop rapide et importante. Des chercheurs de France, Allemagne, Suisse et Russie ont cependant découvert une nouvelle phase dans les électrodes à redox anionique soumises à des tensions élevées, qui améliore leur durabilité. Publiés dans Nature Communications, ces travaux aident à mieux comprendre la redox anionique, avec l’espoir de l’adapter pour des applications à l’échelle industrielle.
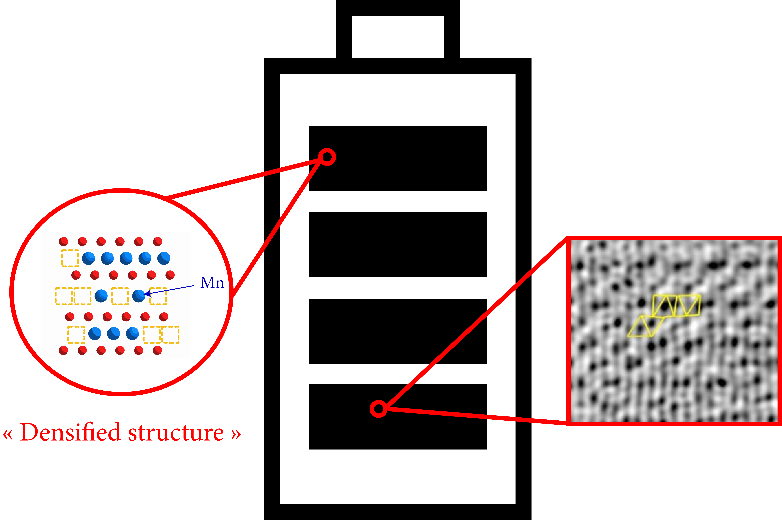
Les piles et les batteries fonctionnent grâce à des échanges d’électrons entre ions positifs (cations) et négatifs (anions) : les réactions d’oxydoréduction (redox). La circulation des électrons permet de stocker ou libérer de l’énergie. Les systèmes redox classiques se focalisent sur l’activité des cations, mais tout un pan de la recherche s’intéresse depuis quelques années aussi aux anions. La redox anionique, qui combine l’activité des deux types d’ions, double les performances énergétiques des piles, mais souffre en retour de chutes intempestives de tension et supporte un plus faible nombre de cycles de charge et décharge. Afin d’amoindrir ces points négatifs en vue d’un développement industriel, une équipe internationale[1] a exploré le comportement d’une électrode type dans de fortes conditions de redox anionique. Les chercheurs ont ainsi découvert une nouvelle phase dans la structure du matériau.
Leur électrode[2] riche en lithium a été soumise à des conditions d’oxydation (4,8 V) et de réduction (1,2 V) plus importantes que celles présentes dans les applications courantes. L’oxydation a formé une nouvelle phase jusqu’à l’intérieur du matériau, alors que l’on pensait que le phénomène n’opérait qu’en surface. Électrons et atomes y circulent ainsi plus efficacement, tandis que l’électrode insère davantage d’ions pendant la réduction. Elle fonctionne ainsi mieux et s’use moins lors de chaque cycle de charge/décharge. L’électrolyte, soit le liquide ionique où sont plongées les électrodes, s’abime cependant davantage. Malgré cela, la stratégie d’oxydation/réduction présentée offre une nouvelle piste pour lever les verrous bloquant le développement commercial de la redox anionique.
Ces travaux ont rassemblé des chercheurs du laboratoire Chimie du solide et de l’énergie (CSE, CNRS/Sorbonne Université/Collège de France), de l’Institut des sciences analytiques et de physico-chimie pour l’environnement et les matériaux (IPREM, CNRS/Université de Pau), de l’Institut de recherche de chimie de Paris (IRCP, CNRS/Chimie ParisTech), tous les trois réunis au sein du Réseau sur le stockage électrochimique de l’énergie (RS2E), ainsi que de l’institut Skolkovo des sciences et technologies (Russie), de l’université technique de Munich (Allemagne) et de l’institut Paul Scherrer (Suisse).

Référence :
Wei Yin, Alexis Grimaud, Gwenaelle Rousse, Artem M. Abakumov, Anatoliy Senyshyn, Leiting Zhang, Sigita Trabesinger, Antonella Iadecola, Dominique Foix, Domitille Giaume & Jean-Marie Tarascon. Structural evolution at the oxidative and reductive limits in the first electrochemical cycle of Li1.2Ni0.13Mn0.54Co0.13O2. Nature Communication, 06/03/20.
