Une avancée vers de nouveaux traitements anti-cancéreux et antiparasitaires
Les endoperoxydes sont des molécules naturelles présentant des propriétés anti-tumorales ou antibactériennes. Hélas, leur synthèse en laboratoire demeure un défi en raison de leur instabilité et du manque de contrôle de la sélectivité. En développant une nouvelle méthode de synthèse, des scientifiques du CNRS sont parvenus à surmonter cet obstacle et à obtenir en laboratoire un endoperoxyde aux propriétés cytotoxiques et anti-parasitaires prometteuses.
Les endoperoxydes sont des produits naturels que l’on retrouve dans des plantes, des organismes marins ou bien encore des microorganismes variés. Ces molécules sont généralement instables et réactives en raison de la liaison O–O fragile et cette propriété est souvent utilisée dans des processus chimiques ou biologiques. Elle peut par exemple induire des réactions de type radicalaire dans les organismes vivants, ce qui en fait des agents potentiellement puissants dans certains traitements antitumoraux ou antibactériens. Ces molécules sont également connues pour jouer un rôle de répulsif ou biocide pour les plantes, d'antifouling pour des éponges ou encore d'antifongique pour certains insectes.
D’où l’intérêt de mieux comprendre le mode de fonctionnement de ces substances naturelles qui jouent un rôle de premier plan pour l’organisme qui les produit. Mais aussi, pourquoi pas, de les produire de manière synthétique, en laboratoire, pour les utiliser dans de nouveaux traitements.
Hélas, du fait de fragilité de la liaison peroxyde, les méthodes actuellement décrites pour synthétiser ces molécules complexes en laboratoire sont relativement peu nombreuses et non stéréosélectives. Ce qui signifie qu’elles conduisent à la formation de plusieurs isomères1 sans favoriser celui que l’on souhaite obtenir. Par exemple, dans le cas de molécules chirales qui présentent deux isomères appelées énantiomères, images l’une de l’autre dans un miroir, il est souvent essentiel d’être capable de ne produire qu’un seul des deux énantiomères.
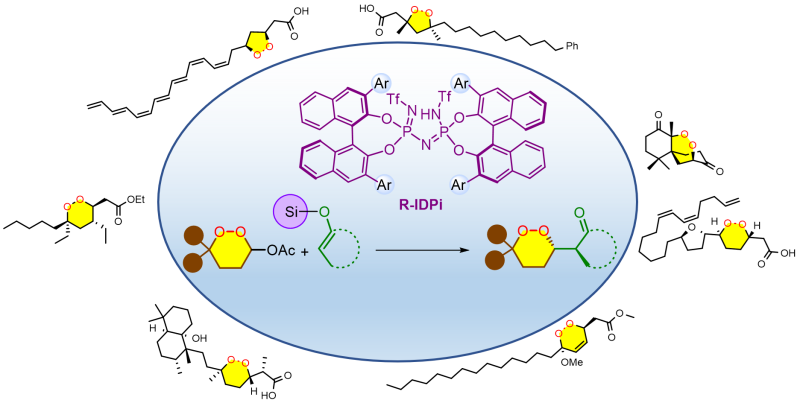
Des scientifiques du laboratoire BioCIS (CNRS/Université Paris-Saclay) ont réussi à mettre au point une réaction pour la synthèse d’endoperoxydes chiraux présentant un haut degré d’énantiosélectivité. Ils ont utilisé pour cela des organocatalyseurs chiraux hautement acides, appelés IDPi, qui permettent la génération d’espèces cationiques réactives dans une poche chirale confinée, à la manière d'une enzyme. Ils sont ainsi parvenus à synthétiser en laboratoire un endoperoxyde naturel, l’ethyl plakortide Z, habituellement extraits d'éponges du genre Plakortis, qui présente des activités cytotoxiques et anti-parasitaires prometteuses.
Rédacteur : CCdM
- 1Un isomère est une molécule qui partage la même formule brute avec une autre, mais qui diffère par la structure ou l arrangement spatial de ses atomes.
Référence
Bastien Champciaux, Nicolas Jamey, Bruno Figadère, and Laurent Ferrié
Peroxycarbenium-Mediated Asymmetric Synthesis of 1,2-Dioxanes and 1,2-Dioxolanes
J. Am. Chem. Soc. 2025
https://doi.org/10.1021/jacs.4c13899