Des complexes bio-inspirés dans le vent
Les complexes inorganiques de synthèse à base de manganèse sont d’excellents candidats pour traiter certaines maladies inflammatoires dues au stress oxydant. Cependant, une fois dispersés dans le milieu biologique, il est très difficile de suivre leur devenir pour comprendre, modéliser et optimiser leur activité biologique. Des chimistes du LBM (CNRS/ENS-PSL/Université PSL/SU), de l’IPREM (CNRS/Université de Pau et des pays de l’Adour), du SMBP (CNRS/ESPCI-PSL) et du CRSA (Centre de recherche de l’hôpital Saint-Antoine, INSERM/SU) viennent de montrer comment la chimie analytique permet enfin d'y parvenir en les séparant grâce à leur taille et à leur résistance au vent dans un flux de gaz. Ces résultats sont à retrouver dans la revue Angewandte Chemie International Edition.
Les complexes inorganiques, composés d’un ligand organique lié à un cation métallique, sont essentiels à la vie. On sait aujourd’hui que les cations métalliques présents au sein de ces complexes, comme le fer au cœur de l’hémoglobine, participent à la plupart des processus fondamentaux du vivant. Ces molécules sont donc de plus en plus utilisées pour des applications biologiques et médicinales, notamment en tant que médicaments (métallomédicaments). Comme les environnements biologiques contiennent naturellement une grande variété d'ions métalliques et de molécules pouvant jouer le rôle de ligand, les métallomédicaments peuvent y subir des échanges de métal ou de ligand qui diminuent leur concentration intracellulaire et/ou peuvent changer la nature de leur activité biologique. Comprendre et prévoir leur comportement en milieu cellulaire est donc clef pour améliorer ou préserver leur activité biologique. Les complexes de manganèse Mn(II) sont particulièrement difficiles à détecter et à quantifier en raison de grande labilité du ligand et de la rapidité des échanges d’ions métalliques auxquels ils participent. La connaissance de la spéciation d'un complexe de Mn(II) ou d'un ion Mn(II), c’est-à-dire des différentes formes chimiques sous lesquelles ils existent dans le milieu cellulaire, est donc à la fois un réel défi et pourtant une information cruciale.
Au sein du Laboratoire des biomolécules (CNRS/ENS-PSL/Université PSL/Sorbonne Université), le groupe multidisciplinaire "Métaux en biologie et homéostasie redox" développe de tels antioxydants synthétiques bioinspirés à base de complexes de Mn(II) qui imitent des enzymes anti-oxydants, les metalloprotéines superoxyde dismutases ou SODs. Ces enzymes font partie de la première ligne de défense cellulaire contre les dommages des espèces réactives issues du dioxygène. Ils ont développé des petites molécules qui miment la SOD à Mn et qui présentent de bonnes activités intrinsèques antioxydantes et anti-inflammatoires sur un modèle cellulaire constitué de cellules épithéliales de l’intestin développé en collaboration avec l’équipe Microbiote, Intestin et Inflammation du Centre de Recherche de l’hôpital Saint-Antoine (SU/INSERM). Malheureusement, les techniques d’analyse classiques comme la spectrométrie de masse ne permettent pas de remonter à la quantité d’ions Mn(II) qui participent réellement à la forme anti-oxydante dans leur modèle.
Dans une étude récemment publiée comme Very Important Publication dans Angewandte Chemie International Edition, en collaboration avec l’Institut des sciences analytiques et de physico-chimie pour l'environnement et les matériaux (CNRS/Université de Pau et des pays de l’Adour) et le laboratoire de Spectrométrie de masse biologique et protéomique (CNRS/ESPCI-PSL), les chimistes du LBM ont utilisé une méthode de séparation des ions qui implique le mouvement des ions poussés par un flux gazeux et retenus par un champ électrique. Cette technique, dite de mobilité ionique, permet de séparer des molécules en fonction de leur taille. Ils ont ainsi démontré qu’il est possible de distinguer les complexes d’un même ligand lié à différents cations métalliques qui ont pourtant des rayons ioniques similaires (typiquement Mn(II), Fe(II), Co(II), Cu(II), Zn(II)). Couplée à la spectrométrie de masse, cette technique leur a permis démontrer et quantifier la présence des mimes dans des cellules intestinales incubées avec les complexes. Ces résultats sont un pas important vers la mise au point de nouveaux métallomédicaments.
Référence
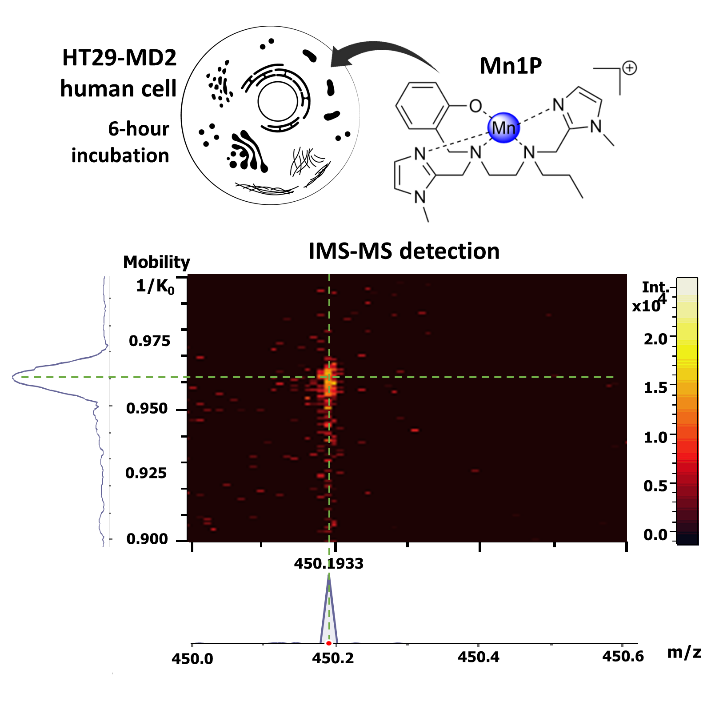
Deciphering the Metal Speciation in Low-Molecular-Weight Complexes by IMS-MS: Application to the Detection of Manganese Superoxide Dismutase Mimics in Cell Lysates, Dr. Martha Zoumpoulaki, Gabrielle Schanne, Dr. Nicolas Delsuc, Dr. Hugues Preud'homme, Dr. Elodie Quévrain, Dr. Nicolas Eskenazi, Géraldine Gazzah, Dr. Regis Guillot, Prof. Philippe Seksik, Dr. Joelle Vinh, Prof. Ryszard Lobinski, Prof. Clotilde Policar, 7 juin 2022
