De l’or pour lutter contre le cancer
Les complexes de métaux précieux jouent un rôle essentiel dans le développement de traitements médicaux, notamment en oncologie. Mais on connaît encore très mal leur mode d’action et leur comportement dans l’environnement biologique. Des scientifiques de l’Institut parisien de chimie moléculaire viennent de réaliser une étude complète de la réactivité chimique et de l'activité antitumorale de divers composés à base d'or, ouvrant ainsi la voie à de nouvelles stratégies thérapeutiques plus efficaces et plus ciblées dans la lutte contre le cancer.
Les métaux précieux comme l’or présentent une structure électronique unique qui leur confère des caractéristiques chimiques exceptionnelles se traduisant par des interactions subtiles avec les molécules biologiques. On retrouve ainsi des complexes à base d’or dans la composition de produits pharmaceutiques comme l’auranofine, un médicament utilisé pour le traitement de l’arthrite rhumatoïde et actuellement en essai clinique comme agent anticancéreux.
Hélas, peu d'informations sont disponibles sur le comportement de ces composés présentant une activité antitumorale dans l’environnement biologique. Se modifient-ils ? Voient-ils leur structure électronique modifiée? Sur quelle partie de la cellule agissent-ils ? Pour tenter de répondre à ces questions, des scientifiques de l’Institut parisien de chimie moléculaire (CNRS/Sorbonne Université)1 viennent de réaliser une étude complète de la réactivité chimique et de l'activité antitumorale de divers composés à base d'or(III).
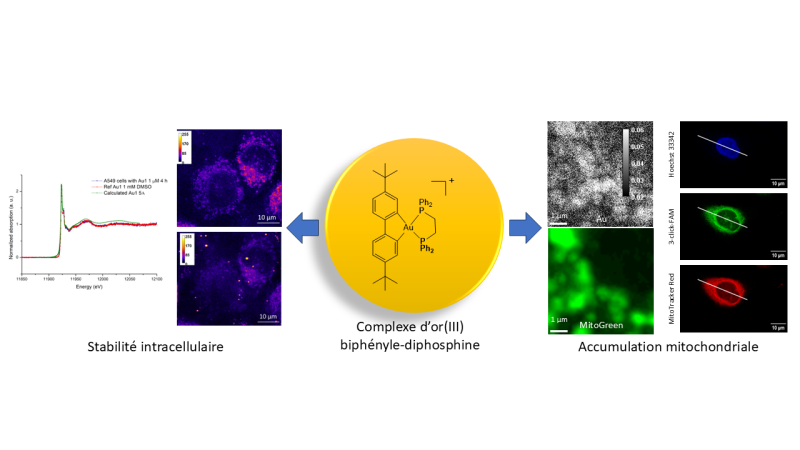
Les composés examinés2 présentent tous une toxicité élevée pour les cellules tumorales. Les analyses, basées sur des techniques spectroscopiques et microscopiques utilisant le rayonnement X produit par un synchrotron, montrent que tous les complexes sont stables à la fois dans des environnements extracellulaires et à l'intérieur de cellules cancéreuses du poumon. Ils ne subissent pas de modification de structure et les atomes d’or restent liés aux ligands. Par microscopie de fluorescence X, les scientifiques sont parvenus à « cartographier » les éléments chimiques, y compris l'or, dans des cellules cancéreuses du poumon hydratées préservées par cryogénisation, avec une résolution de l'ordre de quelques dizaines de nanomètres. L’or s'accumule sélectivement dans les mitochondries, les « centrales électriques » des cellules.
Mieux encore, grâce à une analyse fine par spectroscopie d'absorption des rayons X, les équipes ont obtenu des informations essentielles sur la structure électronique et la géométrie des atomes d'or dans ce milieu biologique. Leurs résultats indiquent que l'activité antitumorale des complexes d'or résulte probablement d'interactions entre les composés dans leur globalité et certaines molécules biologiques spécifiques dont ils perturbent l’activité. Cela représente une différence fondamentale entre ces candidats-médicaments et d'autres complexes antitumoraux à base d'or qui déclenchent généralement la mort cellulaire par coordination directe des atomes d’or avec des biomolécules.
Ces résultats, parus dans la revue Angewandte Chemie, établissent pour la première fois une relation entre la structure chimique et la réactivité d'un complexe d'or, sa spéciation dans la cellule et sa cytotoxicité, ouvrant ainsi de nouvelles pistes pour progresser dans la lutte contre le cancer.
Rédacteur : CCdM
- 1En collaboration avec des scientifiques de l’Institut Néel (CNRS/Université Grenoble Alpes), de l’European Synchrotron Radiation Facility (ESRF), de l’observatoire des sciences de l’univers de Grenoble (CNRS/IRD/INRAE/Météo France/Université Grenoble Alpes) et de l’INSERM.
- 2Complexes cationiques d'or(III) biphényle avec des ligands auxiliaires diphosphine, qui ont en commun un atome d'or lié à deux atomes de carbone du premier ligand et à deux atomes de phosphore du second, s’agrippant comme deux pinces.
Référence
Hester Blommaert, Clément Soep, Edwyn Remadna, Héloïse Dossmann, Murielle Salomé, Olivier Proux, Isabelle Kieffer, Jean-Louis Hazemann, Sylvain Bohic, Michèle Salmain, & Benoît Bertrand
Stability and Mitochondrial Localization of a Highly Cytotoxic Organogold(III) Complex with Diphosphine Ancillary Ligand in Lung Cancer Cells
Angewandte Chemie 2025
https://doi.org/10.1002/anie.202422763