Batteries tout-solide : triple fonction d’un électrolyte pour surpasser les performances de la batterie Li-ion
Grâce à une nouvelle utilisation d’un électrolyte solide à base de lithium, de zirconium et de chlore, les batteries tout-solide pourraient bientôt surpasser les batteries Li-ion tout en étant bien plus sûres. C’est ce que montrent des chimistes du CNRS, en collaboration avec une équipe américaine, dans une étude parue dans le Journal of the Electrochemical Society.
Avec l’arrêt des véhicules thermiques prévu en 2035 et l’électrification progressive de la mobilité, le marché des batteries connaît une croissance exponentielle. Pour l’heure, ce marché repose sur la batterie lithium-ion (Li-ion), technologie phare mais qui atteint ses limites en terme de densité d’énergie. Cette quantité d’énergie qui peut être embarquée par unité de poids de batterie contrôle directement l’autonomie d’un véhicule électrique. Les batteries Li-ion présentent en outre un problème de sécurité puisque le conducteur d’ions entre les deux électrodes de la batterie contient un solvant organique liquide susceptible de s’enflammer en cas de surchauffe de la batterie.
Pour lever ces deux verrous, les scientifiques planchent sur une nouvelle génération de batteries dites « tout-solide ». Ces batteries présentent l’énorme avantage d’utiliser un électrolyte solide comme conducteur ionique entre les électrodes. Ces électrolytes solides en polymère, en composite ou en céramique, permettent en effet de se passer des systèmes de régulation thermique intégrés aux voitures qui sont lourds, coûteux et parfois insuffisants. En terme de densité d’énergie, les batteries tout-solide sont également sur le point de dépasser les batteries Li-ion.
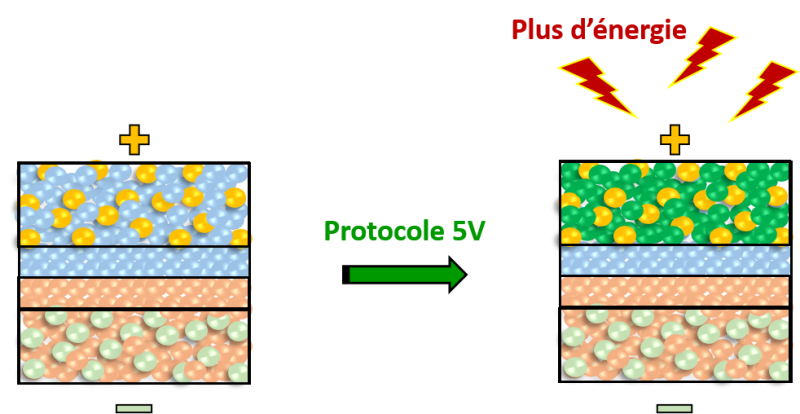
C’est ce que montrent des chimistes de l’Institut des matériaux de Nantes Jean Rouxel (CNRS/Nantes Université) en collaboration avec une équipe de l’Université de Californie à San Diego. Les scientifiques ont découvert deux nouvelles fonctions d’un électrolyte halogéné,* à base de lithium (Li), de chlore (Cl) et de zirconium (Zr). En plus de son rôle de conducteur d’ions, Li2ZrCl6 peut, dans certaines conditions dénommées "protocole 5V", devenir une source supplémentaire d'électrons et d'ions Li pour la batterie. Une partie de ces électrons et ions Li, dite sacrificielle, permet de réparer les déficiences de l'électrode négative, tandis que l’autre partie permet d’augmenter considérablement et durablement la quantité d'électricité qui peut être stockée et restituée par la batterie. L’amélioration des performances a pu être validée pour des cellules-tests de configuration proche de celle des cellules industrielles et pour plusieurs configurations de batterie, certaines ne nécessitant même plus la fabrication de l’électrode négative.
Cette approche novatrice, publiée dans le Journal of the Electrochemical Society, devrait permettre des avancées significatives dans la technologie des batteries tout-solide, plus sûres que les batteries Li-ion. L’équipe de scientifiques démarre à présent une étude approfondie des mécanismes fondamentaux de ces systèmes pour en optimiser le comportement électrochimique dans des batteries réelles.
*Halogéné signifie ici que des ions métalliques sont liés par une liaison ionique à au moins un élément de la famille VII du tableau périodique (les halogènes) : le fluor, le chlore, le brome, l’iode ou l’astate.
Rédacteur: AVR
Référence
Fueling from the Electrochemistry of Halide Solid Electrolytes
Branimir Stamenkovic, Ying Shirley Meng, Philippe Moreau & Joel Gaubicher
Journal of the Electrochemical Society 2024
https://doi.org/10.1149/1945-7111/ad4c99
